根据提供的搜索结果,我们可以了解到关于乙酸乙酯溶解度的一些探究。首先,乙酸乙酯在水中的溶解度随温度的变化而变化。在15℃时,乙酸乙酯在水中的溶解度为8.5g/100***[1][15]。
在探究乙酸乙酯溶解情况的实验中,研究人员使用了饱和碳酸钠溶液、饱和氢氧化钠溶液、饱和碳酸氢钠溶液和水作为溶剂,并分别取4ml溶液进行实验。实验结果显示,碳酸钠、氢氧化钠和碳酸氢钠的溶解度相近,约为5ml,但混合液的体积在静置15分钟后并不相同。实验表明,虽然使用饱和碳酸钠溶液可以降低乙酸乙酯的溶解度,但氢氧化钠也可以达到相似的效果,而饱和碳酸氢钠的效果不如饱和氢氧化钠[2]。
此外,饱和碳酸钠溶液能降低乙酸乙酯在水中的溶解度的原因在于,碳酸钠虽为碱性化合物,但其电离出来的氢氧根浓度不高,无法使反应逆向移动。乙酸乙酯溶于水的一部分很大程度上是靠其中氧和水中氢形成的氢键。当碳酸钠大量溶于水时,占领了一部分氢,由于氢键具有饱和性,自然影响了本来就微溶的油状的乙酸乙酯的溶解度[3]。
关于乙酸乙酯在醇中的溶解度,研究表明,在乙醇中,乙酸乙酯的溶解度为9.8g/100mL;而在甲醇中,乙酸乙酯的溶解度则为25g/100mL左右。总的来说,乙酸乙酯在醇中的溶解度大致呈现随着碳数增加而增大的趋势。这是因为醇分子具有类似于乙酸乙酯的极性结构,它们之间的相互作用力较强,能促进乙酸乙酯在醇中的溶解[8]。
值得注意的是,在70%的乙醇中加入乙酸乙酯,加多少都不会分层。这是因为乙醇与水以任意比例互溶,乙酸乙酯不溶于水。但在这种情况下,溶剂为乙醇(浓度太高),溶剂中又溶了30%的水,乙酸乙酯溶于乙醇,因此不会分层。如果需要分层,可以通过加入乙酸、硫酸并加热的方式,消耗乙醇,最终会出现分层[9]。
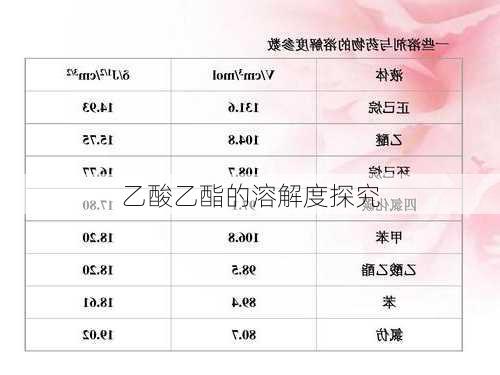
综上所述,乙酸乙酯在不同溶剂中的溶解度受到多种因素的影响,包括温度、溶剂的极性等。通过实验探究和理论分析,我们可以更好地了解乙酸乙酯的溶解度特性。
延伸阅读
参考资料为您提炼了 5 个关键词,查找到 20699 篇相关资料。