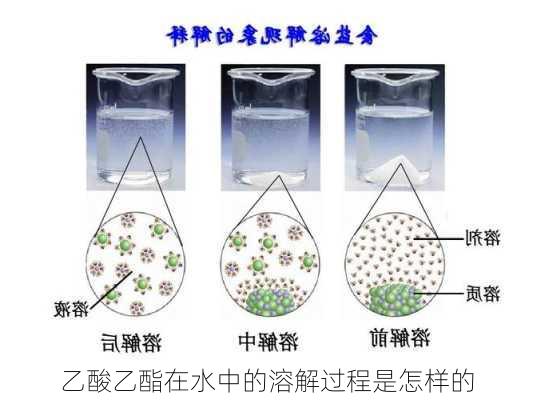
乙酸乙酯在水中的溶解过程
乙酸乙酯在水中的溶解过程是一个复杂的过程,涉及到多个因素,包括温度、压力、溶剂性质等。下面我们将详细介绍这个过程。
1.温度的影响
根据搜索结果,乙酸乙酯在25摄氏度时在水中的溶解度为8.08%。这意味着在常温下,乙酸乙酯能够部分溶解于水中。值得注意的是,随着温度的升高,乙酸乙酯在水中的溶解度可能会降低。这是因为许多物质的溶解度都会随温度的变化而变化,有的物质在低温下溶解度较大,但在高温下溶解度反而减小。
2.溶剂性质的影响
乙酸乙酯是一种非极性分子,而水是一种极性分子。根据相似相溶原理,非极性分子倾向于溶解在非极性溶剂中,而极性分子则倾向于溶解在极性溶剂中。因此,乙酸乙酯在水中的溶解度相对较低。然而,乙酸乙酯在水中能够溶解的一部分程度是由于其中氧原子和水分子之间的氢键作用。
3.水中其他物质的影响
当水中存在其他物质时,如无机盐类,可能会改变乙酸乙酯的溶解度。例如,饱和碳酸钠溶液可以降低乙酸乙酯在水中的溶解度,这是因为碳酸钠能够与水中的氢离子反应,减少了氢键的数量,从而影响了乙酸乙酯的溶解度。
4.溶解平衡
乙酸乙酯的水解是一个可逆反应,其反应方程式为:CH3COOC2H5
+
H2O
→
(可逆)
→
CH3COOH
+
C2H5OH。这意味着在水中,乙酸乙酯会逐渐水解成乙酸和乙醇,同时也会有乙酸和乙醇重新结合生成乙酸乙酯。这种反应过程会在一定条件下达到平衡状态,此时的溶解度就是该物质在这种条件下的饱和溶解度。
综上所述,乙酸乙酯在水中的溶解过程是一个受到多种因素影响的复杂过程。了解这些因素对于控制乙酸乙酯的溶解行为以及优化其在水中的应用具有重要意义。
延伸阅读
参考资料为您提炼了 5 个关键词,查找到 29678 篇相关资料。